NGHIÊN CỨU TÍNH KHẢ THI VỀ CHƯƠNG TRÌNH SÀNG LỌC UNG THƯ CỔ TỬ CUNG TOÀN DIỆN TẠI VIỆT NAM
I. MỤC TIÊU CHUNG
Đánh giá tính khả thi của Chương trình quốc gia về sàng lọc ung thư cổ tử cung tại Việt Nam dựa trên sàng lọc HPV và điều trị.
II. TÓM TẮT
Mặc dù đã có những tiến bộ trong dự phòng ung thư cổ tử cung, bao gồm cả áp dụng các loại vắc-xin có hiệu quả và các xét nghiệm phân tử để xác định nguyên nhân (HPV), ung thư cổ tử cung vẫn làmột trong những nguyên nhân chủ yếu gây bệnh tật và tử vong cho phụ nữ Việt Nam Cơ quan Sáng kiến ung thư toàn cầu (Global Cancer Initiative- GCI) đề xuất hợp tác với tư cách là cố vấn kỹ thuật với Bộ Y tế Việt Nam và các chuyên gia để tiến hành một nghiên cứu khả thitheo mô hình sàng lọc HPV và điều trị (HPV detection-based screen-and-treat – gọi tắt là mô hình HPV S&T) mà sau đó có thể được nhân rộng để thực hiện một chương trình quốc gia sàng lọc ung thư cổ tử cung ở Việt Nam.
Mục tiêu của các nghiên cứu khả thi này là nhằm: 1) tiến hành nghiên cứu tác nghiệp nhằm tìm hiểu các thiếu hụt về mặt năng lực để thực hiện một chương trình quốc gia như trên; 2) đánh giá tính hiệu quả bằng cách sử dụng một yếu tố nguy cơ ung thư, theo tế bào học gọi là tổn thương nội biểu mô vảy ở mức độ cao; 3) đánh giá các chi phí và hiệu quả chi phí của mô hình HPV S &T; và 4) đánh giá các rào cản đối với sự tham gia bằng cách tiến hành một nghiên cứu hồi cứu đối với những phụ nữ đã hoàn thành vào không hoàn thành can thiệp sàng lọc.
III. TỔNG QUAN VÀ CƠ SỞ CỦA VIỆC TIẾN HÀNH NGHIÊN CỨU
Trên toàn cầu, ung thư cổ tử cung là ung thư đứng thứ ba trong số những nguyên nhân gây ung thư ở phụ nữ và gây tử vong liên quan đến ung thư (http://globocan.iarc.fr/). Hơn 500.000 trường hợp ung thư cổ tử cung và gần 300.000 ca tử vong liên quan đến ung thư cổ tử cung xảy ra hàng năm, hầu hết (> 85%) trong số đó xảy ra ở các nước có thu nhập thấp và trung bình (LMIC). Ung thư cổ tử cung thường là nguyên nhân hàng đầu gây tử vong liên quan đến ung thư và nằm trong những nguyên nhân quan trọng nhất của tất cả các nguyên nhân tử vong ở các quốc gia LMIC. Các tác động xã hội của ung thư cổ tử cung là sâu sắc hơn so với hầu hết các bệnh ung thư khác bởi vì bệnh này ảnh hưởng trực tiếp đến phụ nữ, và tại các quốc gia LMIC thường làm dẫn đến tử vong của phụ nữ ở độ tuổi 30, 40, 50, khi họ đang đóng góp nhiều nhất cho gia đình và xã hội. Việt Nam là một trong những quốc gia chịu ảnh hưởngrất lớn của ung thư cổ tử cung, tại Việt Nam, nơi bệnh này được gọi là "dịch hạch của phụ nữ" hoặc "thần chết của phụ nữ".
Tuy nhiên, ung thư cổ tử cung có thể được dự phòng hiệu quả. Việc triển khai các chương trình sàng lọc theo phương phápPapanicolaou (Pap) từ giữa thế kỷ 20 đã làm giảm trên 70% số trường hợp mắc ung thư cổ tử cung ở những quốc gia phương Tâyđã thực hiện hiệu quả chương trình này (1, 2). Tuy nhiên, xét nghiệm Pap có hạn chế do độ nhạy không cao và kết quả thay đổi theo từng lần xét nghiệm, chỉ thực hiện được tại các phòng thí nghiệm chuyên môn (3) và chỉ có thể tái khẳng định kết quả một cách tương đối khi được thực hiện bởi các chuyên gia bệnh học tế bào khác nhau (4). Kết quả là, xét nghiệm Pap phải được thực hiện lặp lại liên tục để đạt được hiệu quả chương trình nhằm ngăn ngừa ung thư cổ tử cung và cần có đầu tư đáng kể để duy trì chất lượng hoạt động (1). Vì vậy, chương trình xét nghiệm Pap là tốn kém để thiết lập và khó khăn để duy trì, và nói chung không bền vững tại các quốc gia LMIC. Như vậy, mặc dù Pap đã được triển khai thành công tại một số khu vực trên thế giới từ 50 năm nay, rõ ràng rằng không phải tất cả các khu vực có thể thực hiện và duy trì chương trình sàng lọc dựa trên Pap. Hiện nay các quốc gia LMIC đang thực hiện các phương pháp đơn giản và dễ thực hiện hơn để đạt được giảm đáng kể tỷ lệ mắc bệnh ung thư cổ tử cung trên toàn cầu và làm giảm sự khác biệt 10 lần trong tỷ lệ mắc ung thư cổ tử cung và tử vong hiện đang tồn tại giữa các quốc gia LMIC và các quốc gia giàu có.
Đầu những năm 1980,việc Harold Zur Hausen (người đoạt giải Nobel Y học, 2008) phát hiện ra virus HPV gây ung thư cổ tử cung đã cách mạng hóa sự hiểu biết của chúng ta về nguyên nhân ung thư cổ tử cung. Trong 30 năm tới, các nhà khoa học thực nghiệm, dịch tễ học, lâm sàng, và y tế công cộng sẽhết sức nỗ lực hợp tác để tìm hiểu cơ chếHPV gây ra ung thư cổ tử cung như thế nào. Hiện nay chúng ta đã biết rằng nhiễm một số chủng loại HPV ở cổ tử cung lànguyên nhân cần thiết và phổ biến của bệnh ung thư cổ tử cung và các tổn thương tiền ung thư (5, 6). Phát hiện ra nguyên nhân gây ra ung thư cổ tử cung đã dẫn đến sự phát triển nhanh chóng của hai tiến bộ công nghệ: 1) vắc xin dự phòng nhiễm HPV để dựphòng sơ cấp và 2) xét nghiệm HPV để xác định những phụ nữ có tổn thương tiền ung thư cần điều trị để dự phòng thứ cấp.
Mặc dù dự phòng bằng tiêm vắc xin phòng HPV có lẽ sẽ là chiến lược dự phòng cuối cùng, đặc biệt là khi thế hệ vắc-xin tiên tiến có tác dụng với 7chủng loại HPV gây ra trên 85% số ca ung thư, đây vẫn không phải là biện pháp vạn năng. Tiêm vắc xin HPV hiện tại chỉ nhắm tới các chủng loại HPV16 và HPV18, gây 70% số ung thư cổ tử cung, và không điều trị được bệnh có từ trước. Vì vậy, ngay cả khi vắc-xin HPV đa hóa trị có ngay lập tức trên phạm vi toàn cầu, vẫn có nhiều thế hệ phụ nữ không được hưởng lợi từ tiêm phòng HPV và tác động của một chương trình tiêm phòng HPV sẽ không thể cảm nhận được trong vòng 20-25 năm. Trong giai đoạn chuyển tiếp, ít nhất 10 triệu phụ nữ trên toàn thế giới sẽ chết vì ung thư cổ tử cung. Vì vậy, dự phòng thứ phát thông qua phát hiện và điều trị các tổn thương tiền ung thư và ung thư giai đoạn đầu sẽ là giải pháp trước mắt để giảm bớt gánh nặng của bệnh ung thư cổ tử cung.
Xét nghiệm phân tửHPV có độ nhạy cao hơn (3, 7-11) và độ tin cậy cao hơn để phát hiện các tổn thương tiền ung thư của cổ tử cung hơn so với xét nghiệm Pap. Độ nhạy của xét nghiệm phân tử HPV cao hơn so vớixét nghiệm Papcó hai lợi ích quan trọng: 1) phát hiện sớm các tổn thương tiền ung thư nếu được điều trị sẽ dẫn đến giảm tỷ lệ mắc ung thư cổ tử cung trong vòng 4-5 năm (9, 10) và giảm tử vong có liên quan trong vòng 8 năm (12) và 2) một sự bảo đảm đối với nguy cơ ung thư (nguy cơ ung thư thấp hơn) trong nhiều năm sau khi đạt kết quả xét nghiệm âm tính (13, 14). Điều này cho phép một khoảng thời gian dài 5-10 năm không phải sàng lọc lại, tùy thuộc vào sự chấp nhận của xã hội đối với nguy cơ ung thư. Vì vậy, sử dụng xét nghiệm phân tử HPV, người phụ nữ chỉ cần một hoặc một vài lần sàng lọc trong suốt cuộc đời, làm giảm đáng kể gánh nặng của ung thư cổ tử cung (15). Xét nghiệm phân tử HPVcó các lợi thế quan trọng khác bao gồm cả độ tin cậy và thực hiện dễ dàng hơn bởi vì các xét nghiệm phân tử không yêu cầu đào tạo chuyên ngành sâu về y tế. Những lợi thế này làm cho việc triển khai xét nghiệm phân tử HPV đểsàng lọc ung thư cổ tử cung vào các quốc gia LMIC là mang tính khả thi.
Dựa trên các bằng chứng áp đảo rằngxét nghiệm HPV là đáng tin cậy, có độ nhạy cao hơn và chu kỳ an toàn dài hơn sau khi có kết quả xét nghiệm âm tính, một số quốc gia hoặc chuyển đổi từ xét nghiệm Pap sang xét nghiệm HPV (hoặc thêm xét nghiệm HPV để bổ sung cho chương trình Pap); hoặc trong trường hợp trước đây chưa từng cóchương trình Pap thì triển khai luôn xét nghiệm HPV ngay từ đầu. Những quốc gia này bao gồm (danh sách chưa đầy đủ):
.png)
Các chương trình sàng lọc ung thư cổ tử cung theo cách cổ điển đã kết hợp chẩn đoán khẳng địnhbằng soi cổ tử cung và sinh thiếtnhằm ra quyết định xử trí, và theo dõi của những phụ nữ màchẩn đoán mô học chưa khẳng định tổn thương tiền ung thư cổ tử cung (ví dụ, tân sản trong biểu mô cổ tử cung độ 2 [CIN2] hoặc độ 3 [CIN3]) hoặc ung thư (CIN2 +). Tuy nhiên, trong khi các bước này làm tăng thêm tính đặc hiệu cho chương trình bằng cách xác định chính xác hơn cácphụ nữ với + CIN2, chúng cũng đồng nghĩa với việc gia tăng chi phí đáng kể, nhu cầu cơ sở hạ tầng, và giảm độ nhạy đối với CIN2 + vì các sai sót trong chương trình như phân loại bệnh sai và mất dấu các phụ nữ được sàng lọc dương tính để theo dõi hoặc thực hiệncác bướclâm sàng tiếp theo. Các chiến lược mới thay thế cho cách cổ điểnđã đơn giản hóa quy trình kỹ thuật,tạo một sự cân bằng giữa lợi ích và tác hại, đồng thời giảm các chi phí trực tiếp và gián tiếp, do đó làm cho chương trình có tính khả thi cao trong điều kiện nguồn lực hạn chế.
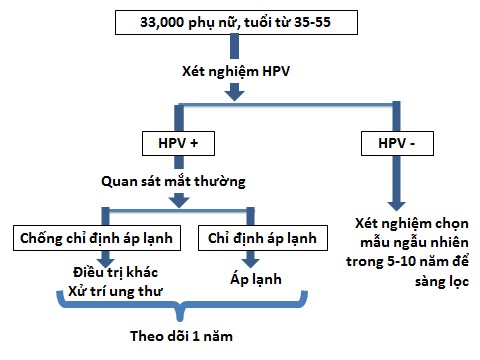
Sàng lọc HPV và điều trị(HPV S & T) là một chiến lược đơn giản đã được chứng minh có hiệu quả. Trong HPV S & T, đầu tiên, người phụ nữ được sàng lọc bằng cách lấy bệnh phẩm cổ tử cung và xét nghiệm DNA của HPV gây ung thư. Phụ nữ có kết quả HPV âm tínhcoi như được sàng lọc xong và nhiều năm sau, theo quy ước, mới cần tái sàng lọc. Phụ nữ có kết quả xét nghiệm HPV dương tính cần được đánh giá bằng mắt thường (VE) để xem xét điều trị áp lạnh. Những phụ nữ có chống chỉ định điều trị được chuyển tuyến đến bệnh viện khu vực hoặc BV trung ương để chẩn đoán và điều trị các tổn thương tiền ung thư lớn bằng phẫu thuật và điều trị ung thư bằng cắt bỏ tử cung hoặc xạ trị.
Phương pháp áp lạnh là một phương pháp bóc tách điều trị các tổn thương cổ tử cung bằng cách đóng băng biểu mô và giết chết các tế bào bao gồm cả những tế bào bị nhiễm HPV. Phương pháp áp lạnh áp dụng cho bệnh nhân ngoại trú, là phương pháp điều trị đơn giản mà bất kỳ cán bộ y tế được đào tạo nào cũng có thể thực hiện. Đó là phương pháp tương đối lành tính, chỉ gây ra tác dụng phụchủ yếu là tiết dịch âm đạo (tróc các tế bào chết) trong 30 ngày tiếp theo sau khi điều trị. Mặc dù, tỷ lệ biến chứng của phương pháp áp lạnh thấp, phụ nữ sẽ được phát thêm tài liệu để theo dõi các dấu hiệu nguy cơ và được hướng dẫn để tái khám nếu các dấu hiệu này xảy ra.
Ở Nam Phi, trong một dân số có nguy cơ cao bao gồm một tỷ lệ lớn phụ nữ nhiễm HIV, một chu kỳ thực hiện HPV S & T làm giảm 75%tỷ lệ mắc CIN2+ trong vòng ba năm theo dõi (16). Cũng đáng chú ý rằng phụ nữ có xét nghiệm HPV dương tính tại một thời điểm có nguy cơ cao của CIN2 + ở giai đoạn 18 năm sau so với những phụ nữ có HPV âm tính (14). Vì vậy, điều trị nhiễm HPV không kèm theo + CIN2 đồng thời sẽ làm giảm nguy cơ tương lai của CIN2 + trong nhiều thập kỷ.
Việt Nam là quốc gia Đông Nam Á đang có tăng trưởng kinh tế cao, từ một trong những nước nghèo nhất trên thế giới thành một quốc gia có thu nhập trung bình thấp (http://www.worldbank.org/en/country/vietnam). Mặc dù có những tiến bộ kinh tế, các chương trình phòng chống ung thư, kiểm soát, và chăm sóc chưa được triển khai tốt. Tỷ suất mới mắc ung thư cổ tử cung toàn quốc hàng năm là tương đối thấp (http://globocan.iarc.fr/), dưới đây là kịch bản được dự đoán dựa trên tình trạng kinh tế trước đây, và dựa trên việc thiếu sàng lọc toàn diện, có lẽ vì thiếu giám sát trọng điểm bệnh, đặc biệt là ở các vùng nông thôn, vùng sâu vùng xa. Một báo cáo cho thấy 5.000 phụ nữ được chẩn đoán mắc bệnh ung thư cổ tử cung và 2,500 phụ nữ tử vong do ung thư cổ tử cung mỗi năm. Mặc dù chưa cócác số liệu thống kê chính xác về sàng lọc ung thư cổ tử cung, hàng năm tại Việt Nam tiến hành khoảng gần 500.000 Pap với chất lượng chưa được khẳng định, trong khi toàn quốc có hơn 40 triệu phụ nữ, bao gồm> 10 triệu phụ nữ trong độ tuổi từ 35 và 55 tuổi là những người cần sàng lọc. Vì vậy, rất có thể là quy mô của bệnh ung thư cổ tử cung tại Việt Nam đang được đánh giá thấp. Việt Nam cần có một chương trình sàng lọc toàn diện được phổcập rộng rãi.
Theo thỏa thuận với Bộ Y tế Việt Nam (BYT), các tổ chức bao gồm: Sáng kiến ung thư toàn cầu (GCI), ILSBio, LLC và các tổ chức khác của Hoa Kỳ có kế hoạch hợp tác với Bộ Y tế với tư cách là các đối tác kỹ thuật để tiến hành một nghiên cứu tính khả thi để đánh giá sự phù hợp của việc thực hiện một chương trình sàng lọc ung thư cổ tử cung quốc gia dựa trên HPV S & T tại Việt Nam.
- Mục tiêu cụ thể của đề xuất nghiên cứu
1) Đánh giá sự thiếu hụt trong năng lực (ví dụ, tìm dấu bệnh nhân và theo dõi, bệnh học, lấy bệnh phẩm, xử lý, vận chuyển và lưu trữ; và lâm sàng và thực hành trong phòng thí nghiệm, vv) cần thiết để thực hiện HPV S & T trên toàn quốc.
2) Đánh giá các rào cản chương trình đối với việc thực hiện (ví dụ như giáo dục nâng cao sức khỏe, đào tạo, và sự tham gia và tỷ lệ hoàn thành).
3) đánh giá tính hiệu quả bằng cách sử dụng một yếu tố nguy cơ ung thư, theo tế bào học gọi là tổn thương nội biểu mô dạng vảy ở mức độ cao giải thích như là cao cấp vảy biểu mô tổn thương (high-grade squamous intraepithelial lesions-HSIL)bằng cách đánh giá phụ nữ trước và sau khi sự can thiệp S & T HPV.
4) Đánh giá các chi phí và chi phí- hiệu quảcủa HPV S & T.
5) đánh giá các rào cản đối với sự tham gia bằng cách tiến hành một nghiên cứu hồi cứu đối với những phụ nữ đã hoàn thành vào không hoàn thành can thiệp HPV S & T.
.
6) thiết lập giám sát trọng điểm đối với phụ nữ có kết quả sàng lọc âm tính nhằm đánh giá sự an toàn lâu dài và xác định các khoảng thời gian tái sàng lọc thích hợp.
IV. Tiếp cận và phương pháp
Các trung tâm nghiên cứu lâm sàng và đối tượng dân số đích.Đây là đề xuất một nghiên cứu khả thi sử dụng HPV S & T trên 33.000 đối tượng phụ nữ, tuổi từ 35-55. Đối tượng phụ nữ sẽ được lựa chọn ngẫu nhiên thông qua việc sử dụng tổng điều tra dân số. Phụ nữ sẽ tham gia làm đối tượng nghiên cứu tại 3 trung tâmnghiên cứu lâm sàng tại Hà Nội, thành phố Hồ Chí Minh và Huế. Bệnh phẩm sẽ được thu thập tại 3 trung tâm trên và tại một số địa bàn nghiên cứuriêng lẻ khác, theo tỷ lệ xấp xỉ bằng nhau (~ 11.000 cho mỗi trung tâm). Trung tâm tại Huế sẽ chịu trách nhiệm điều phối đối với các địa bàn nghiên cứu riêng lẻ. Tiêu chuẩn tham gia bao gồm: không có thai (đối tượng tự báo cáo), chưa từng trải qua phẫu thuật cắt tử cung, và có đủ nhận thức để ký bản đồng ý tham gia có hiểu biết (informed consent). Các phụ nữ đã ký bản đồng ý tham gia sẽ được ghi danh vào nghiên cứu.
Thăm khám lấy bệnh phẩm.Đối tượng phụ nữ đủ tiêu chuẩn và đã ký bản đồng ý sẽ trải qua lần thăm khám lấy bệnh phẩm; những phụ nữ đang ở trong thời kỳ kinh nguyệt sẽ được hoãn lại hai tuần. Tại phòng khám hoặc phòng tư vấn, phụ nữ đủ tiêu chuẩn và đã ký bản đồng ý được y tá / nữ hộ sinh yêu cầu điền một bảng kiểm ngắn về thông tin chung và các yếu tố nguy cơ. Sau đó, trong phòng thủ thuật, tiến hành lấy bệnh phẩmâm đạo - cổ tử cung không cần sử dụng mỏ vịt, bằng cách sử dụng chổi lấy bệnh phẩm đơn giản do tổ chức Dự phòng Ung thư Quốc tế thiết kế (Cleveland, OH, Hoa Kỳ), tương tự như dụng cụ lấy bệnh phẩm của hãng Qiagen (Gaithersburg, MD, Hoa Kỳ). Các bệnh phẩm thu được sẽ được đặt trong dung dịch bảo quản và gửi đến phòng thí nghiệm lâm sàng tại Hà Nội để tiến hành xét nghiệm HPV. Một mẫu thứ hai sẽ được thu thập ngẫu nhiên theo cùng một cách và đặt trên thẻ bảo quản khô (FTA Elute GE Healthcare) nhằm mục đích đánh giá hình thức bảo quản bệnh phẩm bằng thẻ FTA. Nghiên cứu thí điểm sử dụng thẻ FTA để xét nghiệm HPV đã cho kết quả rất hứa hẹn của thẻ này (17-20) (Guan và cộng sự, công trình chuẩn bị công bố), nhưng vẫn cần có một đánh giá lớn hơn, nghiêm ngặt hơn trước khi sử dụng thẻ FTA trong bảo quảnbệnh phẩmmột cách thường quy. Mẫu bệnh phẩm bảo quản trên thẻ FTAsẽ được gửi đến một phòng thí nghiệm nghiên cứu của Hoa Kỳ để đánh giá nhưng kết quả sẽ không được sử dụng cho việc ra quyết định lâm sàng.
Theo dõi các phụ nữ có kết quả sàng lọc dương tính. Phụ nữ có kết quả xét nghiệm HPV dương tính sẽ được chuyển đến trung tâm nghiên cứu lâm sàng gần nhất để đánh giá và xử trí lâm sàng. Đối tượngHPV dương tính sẽ được khám vùng chậu theo phương pháp chuẩn bằng cách sử dụng mỏ vịt do y tá / nữ hộ sinh thực hiện. Đầu tiên, bệnh phẩm cổ tử cung sẽ được thu thập bằng cách sử dụng dụng cụ lấy bệnh phẩm Cervex Broom (hãng Rovers) và bảo quản bằng PreservCyt (hãng Hologic, Bedford, MA, USA). Mẫu bệnh phẩm này này sẽ được sử dụng để làm tiêu bản ThinPrep (hãng Hologic) để đánh giá tế bào học. Tiếp theo, cổ tử cung sẽ được bôi axit axetic loãng để được kiểm tra bằng mắt thường tổn thương màu trắng (acetowhite) để xác định phụ nữ có HPV dương tính này có đủ điều kiện để làm áp lạnh. Phụ nữ có tổn thương acetowhite rộng hoặc không thể nhìn rõ, hoặc có ung thư rõ ràng, hoặc có chống chỉ định khác sẽ được chuyển đê tiếp tục đánh giá, chẩn đoán, và điều trị thích hợp. Một trung tâm lâm sàng sẽ được trang bị máy soi cổ tử cung kỹ thuật số có độ phân giải cao để ghi lại hình ảnh của cổ tử cung và tạo ra một thư viện kỹ thuật số cho các mục đích tập huấn và đào tạo. Phụ nữ không có chống chỉ định sẽ được thực hiện áp lạnh bằng cách sử dụng một súng lạnh được làm lạnh bằng khí N20 theo phác đồ 3'-5-'3 '.
Tất cả các phụ nữ HPVdương tính sẽ được theo dõi một năm, trừ những người được chẩn đoán mắc ung thư (và do đó được chăm sóc đặc biệt) để đo lường tác động của can thiệp và để đảm bảo sự an toàn cho những phụ nữ có nguy cơ cao. Đầu tiên sẽ thu thập mẫu bệnh phẩmâm đạo cổ tử cung đểxét nghiệm HPV, tiếp theo là khám phụ khoa kèm theo thu thập bệnh phẩm cổ tử cung bằng ThinPrep cho tế bào học và quan sát bằng VIA. Phụ nữ có tổn thương acetowhite bằng mắt thường, hoặc sau đó được xác định là HPV dương tính, hoặc có tế bào học HSIL sẽ được chuyển để tiếp tục đánh giá lâm sàng và điều trị.
Theo dõi lâu dài phụ nữ sàng lọc âm tính. Để giám sát mức độ an toàn của phụ nữ HPVâm tính và để đề xuất với Bộ Y tế về cácphương án quy định khoảng thời gian cần tái sàng lọc (nếu phụ nữ lựa chọn tái sàng lọc), hàng năm, một nhóm 2.000 phụ nữ HPVâm tính sẽ được lựa chọn ngẫu nhiên trong vòng từ 5 đến 10 năm theo dõi. Như đã mô tả ở trên, một mẫu bệnh phẩm âm đạo cổ tử cung sẽ được thu thập từ toàn bộ nhóm phụ nữ được chọn mẫu và đối với các phụ nữ HPV dương tính, bệnh phẩm cổ tử cung sẽ được thu thập tại thời điểm quan sát bằng VIA.
Xét nghiệm HPV. Bệnh phẩmâm đạo cổ tử cung được thu thập ban đầu và sau một năm theo dõi (đối với những phụ nữlần đầu có kết quả HPV dương tính) sẽ được xét nghiệm HPV gây ung thư bằng cách sử dụng Cobas4800 (công ty Roche Molecular System, Pleasanton, CA, USA) (11). Xét nghiệm HPV Cobas4800 là xét nghiệm real-time PCR cho kết quả riêng biệt đối với HPV16, HPV18, và kết quả chung cho cả nhóm 11 kiểu gen HPV gây ung thư cộng với HPV66. Xét nghiệm HPV Cobas4800 HPV cũng đánh giá tính phù hợp của bệnh phẩm bằng định lượng globin b. Các mẫu bệnh phẩmâm đạo cổ tử cung được thu thập ban đầu và sau 1 năm theo dõi đối với phụ nữ HPV-dương tính, và bệnh phẩm cổ tử cung tương ứng của phụ nữ HPV dương tính ở lần theo dõi; và một mẫu ngẫu nhiên với số lượng tương đương sẽ được thực hiện tại một phòng thí nghiệm khác, cao cấp hơn. Bệnh phẩm sẽ được tái xét nghiệm với số lượng nhỏ theo từng đợt trong suốt quá trình nghiên cứu nhằm giám sát chất lượng phòng thí nghiệm lâm sàng của Việt Nam.
Tế bào học. Các bệnh phẩmđược bảo quản PreservCyt sẽ được gửi đến một phòng thí nghiệm cao cấp của Hoa Kỳđược chọn ký hợp đồng để làm tiêu bản và đánh giá các tế bào học ThinPrep. Các tiêu bản tế bào học sẽ được đọc độc lập với bất kỳ dữ liệu nào nghiên cứu. Kết quả tế bào học sẽ được báo cáo theo phân loại Bethesda 2001 đối với tế bào học cổ tử cung (21): âm tính đối với tổn thương biểu mô vảy (SIL) hoặc ác tính ("âm tính"), các tế bào vảy không điển hình có ý nghĩa không xác định (ASC-US), SIL cấp độ thấp (LSIL), SIL cấp độ cao (HSIL), các tế bào vảy không điển hình không thể loại trừ HSIL (ASC-H), và ung thư. Các nhà bệnh học tế bào sẽ được giao nhiệm vụ tiếp tục phân biệt giữa HSIL thể nặng và nhẹ, HSIL-CIN3 và HSIL-CIN2 tương ứng. Hai nhà bệnh học tế bào sẽ đọc tiêu bản một cách riêng biệt và cùng rà soát kết quả để thống nhất kết quả.
Tập huấn thiết lập nghiên cứu. Chúng tôi đề xuất ký hợp đồng phụ với các cộng tác viên / đối tác sau đây để hỗ trợcho việc thiết lập nghiên cứu:
A. Dịch tễ học/ hậu cần cho thực địa: Tiến sĩ Ana Cecilia Rodriguez, Proyecto Epidemiológico Guanacaste, Fundación Instituto Costarricense de Investigación y Enseñanza en Nutrición y Salud, San José, Costa Rica; Tiến sĩ Fang-Hui Zhao, Viện Ung thư của Viện Hàn lâm Khoa học Trung Quốc, Bắc Kinh, Trung Quốc.
B. Khám VIA / Áp lạnh: Tiến sĩ Jose Jeronimo, Chương trình Công nghệ thích hợp trong y tế (PATH), Seattle, WA, Hoa Kỳ; Basic Health International
C. Soi cổ tử cung và điều trị tổn thương tiền ung thư: Hiệp hội Soi cổ tử cung và bệnh học cổ tử cung Hoa Kỳ (ASCCP)
D. Xử trí ung thư: Tiến sĩ Walter Kinney, Kaiser Permanente Bắc California (KPNC), Tiến sĩ Kathleen Schmeler, Trung tâm Ung thư MD Anderson, Hội Ung Thư phụ khoa (SGO).
E. Bệnh học: Tiến sĩ Mark Stoler, Đại học Virginia (Charlottesville, VA, USA)
F. Thiết lập Phòng thí nghiệm và Quy trình vận hành chuẩn (SOP): Công ty Roche Molecular System; đang tìm người
G. Hệ thống thông tin:đang tìm người
H. Xây dựng tài liệu giáo dục truyền thông:đang tìm người
Phân tích. Mục đích chính cuối cùng của nghiên cứu là đánh giá tính khả thi thông qua việc hoàn thành can thiệp theo từng bước. Để xác định chỉ tiêu theo dõi việc hoàn thành nghiên cứu, chúng tôi sẽ làm việc với Bộ Y tế Việt Nam để xây dưng một Quy trình vận hành chuẩn (SOP) cho nghiên cứu, trong đó sẽ bao gồm các khoảng thời gian cho phép để thực hiện từng bước một cách hợp lý và những tiêu chuẩn hợp lý về tỷ lệ hoàn thành. Chỉ tiêu theo dõi % việc hoàn thành nghiên cứu sẽ được đánh giá tức thời qua một ứng dụng trên internet sẽ được thiết kế riêng cho nghiên cứu này.
Để đánh giá tác động trên bệnh nhân, chúng tôi sẽ sử dụng HSIL hoặc (HSIL +) phát hiện bằng tế bào học trước và sau khi điều trị để đại diện cho tiền ung thư và ung thư cổ tử cung (CIN2 +). Chúng tôi sẽ làm cho các giả định sau: 1) Hầu hết phụ nữ CIN2 + sẽ được xác định là HPV dương tính; 2) HSIL + là một dấu hiệu cụ thể của CIN2 +. Khoảng một nửa HSIL + bằng tế bào học sẽ có tổn thương CIN2 + trên mô học (PPV ~ 50%) và khoảng 1/4 đến 1/3 của mô học CIN2 + sẽ có đồng thời HSIL + tế bào học (đọc bởi một phòng thí nghiệm cao cấp); và 3) Sự phục hồi các tổn thương CIN2 + liên quan với HSIL + tế bào học là rất khó xảy ra trong khoảng thời gian một năm.
Chúng tôi sẽ so sánh % HSIL+ trên tế bào học (bất kỳ HSIL+, HSIL + quy ước, bất kỳ HSIL-CIN3 +, và HSIL-CIN3 + quy ước) ở phụ nữ HPV-dương tính trước khi và sau khi điều trị bằng cách sử dụng một phiên bản chính xác kiểm định chi-bình phương NcNemar trên toàn bộ nhóm phụ nữ tham gia và và phân tầng theo địa điểm trung tâm nghiên cứu và tuổi khi tham gia nghiên cứu. Chúng tôi cũng sẽ so sánh sự phân bố của tất cả các kết quả tế bào học xếp theo trật tự nguy cơ ung thư (ung thư> HSIL-CIN3, HSIL-CIN2, ASC-H, LSIL, ASC-US, và NILM) trước và sau khi sử dụng một phiên bản chính xác của kiểm định chi-bình phương đối xứng. Tỷ lệ của bất thường tế bào học sẽ được xác định bằnggiá trịước tính và khoảng tin cậy 95% (95% CI).
Chúng tôi sẽ báo cáo tỉ lệ lưu hành HPV cụ thể theo tuổi và khoảng tin cậy 95% theo từng trung tâm nghiên cứu. Chúng tôi sẽ đánh giá việc giảm tỷ lệ lưu hành HPV sau khi điều trị, được xem là trị số độc lập với tuổi, khác với tỷ lệ khỏi bệnh được xem là phụ thuộc nhiều vào tuổi, như là một chỉ số thứ cấp của việc điều trị thành công.
Chúng tôi sẽ tính toán các số liệu thống kê chuẩn (Kappa, phần trăm dầu thô thỏa thuận, phần trăm thỏa thuận tích cực, và NcNemar kiểm tra chi-square) xét nghiệm HPV trong các tập hợp con được tái thử nghiệm của Phòng thí nghiệm QC.
Chúng tôi cũng sẽ tiến hành một phân tích mô phỏng tác động của điều trị nếu điều trị đã được thực hiện ngay lập tức cho phụ nữ có xét nghiệm dương tính với HPV16 hoặc HPV18, hai loại HPV gây ung thư nhất gây ra tới 70-75% của tất cả các ung thư cổ tử cung, ngay từ khi có kết quả xét nghiêm Cobas4800. Trong mô phỏng, những người phụ nữ có xét nghiệm HPV dương tính nhưng âm tính với HPV16 và HPV18 sẽ được kiểm tra thêm một lần nữa trong một năm và điều trị nếu có kết quả HPV dương tính.
Chúng tôi sẽ ký hợp đồng phụ với Tiến sĩ Jane Kim, chuyên gia phân tích kinh tế tại Đại học Harvard, để tiến hành phân tích chi phí và hiệu quả chi phí của các kết quả của nghiên cứu khả thi. Chúng tôi cũng sẽ ký hợp đồng phụ với Tiến sĩ Isabel Scarinci, chuyên gia tâm lý học lâm sàng và là chuyên gia về đánh giá các yếu tố quyết định hành vi trong tham gia sàng lọc ung thư. Cả hai dữ liệu sẽ thông báo cho Bộ Y tế về việc làm thế nào để điều chỉnh hoặc cải thiện chương trình quốc gia về HPV S & T tại Việt Nam.
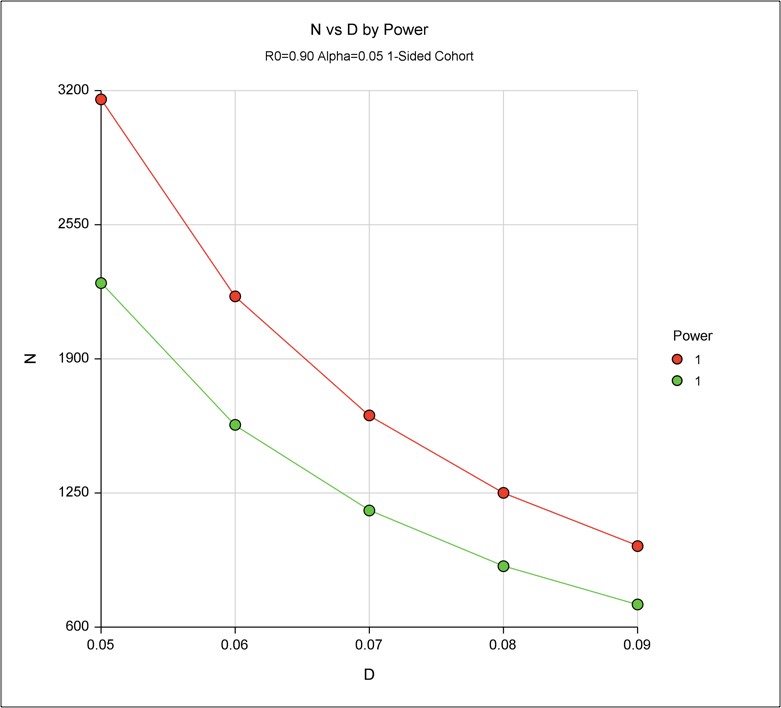
Cỡ mẫu. Để xác định kích thước mẫu của nghiên cứu, chúng tôi sử dụng một cách tiếp cận Post-Marketing Surveillance Power Analysis (PASS) để mô hình hóa tác động của số lượng phụ nữ không có HSIL trên tế bào học trước và sau khi điều trị. Trên cơ sở giả định là 90% phụ nữ HPV dương tính không có đồng thời HSIL trên tế bào học và chúng tôi muốn đánh giá khả năng can thiệp để tăng tỷ lệ này lên trên 90%. Nếu tỷ lệ lưu hành HPV trong quần thể nghiên cứu này là 5%, một quần thể32.520 phụ nữ sẽ có 1.626 phụ nữ HPV dương tính, một cỡ mẫu đủ để đạt được 90% độ nhạy của nghiên cứu (alpha = 0,05) để phát hiện số lượng phụ nữ không có HSIL trên tế bàotăng từ 90% lên tối thiểu 97%. Như vậy, ta sẽ có ít nhất 90% xác suất để phát hiện hiệu quả 70% hoặc cao hơn. Nếu tỷ lệ lưu hành HPV là 10%, một quần thể 31.570 phụ nữ sẽ có 3.157 HPV phụ nữ dương tính, một cỡ mẫu đủ để đạt được 90% độ nhạy của nghiên cứu (alpha = 0,05) để phát hiện một số phụ nữ không có HSIL trên tế bào học tăng từ 90% lên tối thiểu là 95%. Như vậy, ta sẽ có 90% xác suất để phát hiện hiệu quả 50% hoặc cao hơn. Xem Phụ lục 3 về các đồ thị xác suất.
V. Kế hoạch nghiên cứu
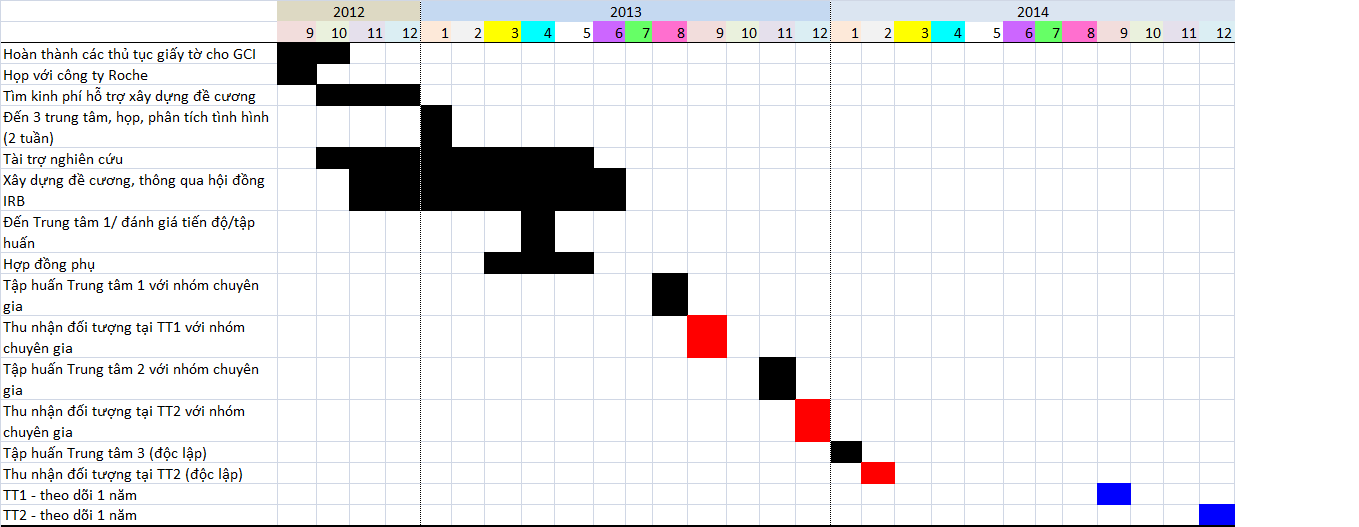
Phụ lục 1: Nhân sự chủ chốt
Bộ Y tế Việt Nam
PGs. Ts. Nguyễn Viết Tiến
Thứ trưởng Bộ Y tế Việt Nam
Ban Quản lý Chương trình - Bộ Y tế
Ts. Nguyễn đức Vinh
Trưởng Bệnh học
Bệnh viện Phụ sản Trung ương
Gs. Ts. Nguyễn Công Khẩn
Cục trưởng, Cục Khoa học, Công nghệ và Đào tạo
Bộ Y tế
Cố vấn Chương trình (Dự kiến)
Gs. Nguyễn Chấn Hùng
Chủ tịch Hội Ung thư Việt Nam
Gs. Ts. Nguyễn Sào Trung
Trưởng Bộ môn Bệnh học
Đại học Y DượcHồ Chí Minh
Ts. Huỳnh Quyết Thắng
Trưởng Bộ môn Ung thư
Trường Đại học Y Cần Thơ
Phó Chủ tịch Hội Ung thư Việt Nam
Đại sứ về Ung thư của Việt Nam
Le Quang Thanh, MD, MSc.
Director of Tu Du O/G hospital
HCMC - Viet Nam
Ts. Bùi Đức Phú
Giám đốc Bệnh viện Trung ương Huế
Ts. Nguyễn Văn Bằng
Trưởng khoa Bệnh học
Bệnh viện Trung ương Huế
Bs. Nguyễn Phi Hùng
Khoa Bệnh học
Viện Ung thư Quốc gia Việt Nam
Bs. Nguyễn Văn Thành
Trưởng khoa Bệnh học
Trung tâm Ung thưTP Hồ Chí Minh
Bà Phan Thị Hạnh,
Chủ tịch, Hội Hộ sinh Việt Nam - Huế
Sáng kiến Ung thư toàn cầu và ILSBio (Global Cancer Initiative and ILSBio)
Richard Thorp
Giám đốc điều hành / Đối tác Quản lý, ILSbioLLC
Cựu Giám đốc Học liệu, Bộ Cựu Chiến binh
Nguyên Phó Giám đốc Truyền thông Cục An ninh xã hội
Gs. Howard Sussman
Giáo sư Bệnh học
Đại học Stanford
Giám đốc khoa học, ILSbioLLC
Ts.Philip E. Castle
Giáo sư thỉnh giảng, Đại học Y khoa Albert Einstein
Phụ lục 2: Thuật toán lâm sàng
Phụ lục 3: Đường Power / Cỡ mẫu
Trong đó N là số lượng phụ nữ HPV-dương tính và D là sự gia tăng trong HSIL-phụ nữ trên 0,90. Đường màu đỏ đại diện cho power 90%, màu xanh lá cây đại diện power 80%.
Tài liệu tham khảo
(1) Kitchener HC, Castle PE, Cox JT. Chapter 7: Achievements and limitations of cervical cytology screening. Vaccine 2006 Aug 21;24 Suppl 3:S63-70.:S63-S70.
(2) Cervix Cancer Screening. IARC Press, 2005.
(3) Cuzick J, Clavel C, Petry KU, et al. Overview of the European and Khôngrth American studies on HPV testing in primary cervical cancer screening. Int J Cancer 2006 Sep 1;119(5):1095-101.
(4) Stoler MH, Schiffman M. Interobserver reproducibility of cervical cytologic and histologic interpretations: realistic estimates from the ASCUS-LSIL Triage Study. JAMA 2001 Mar 21;285(11):1500-5.
(5) Wright TC, Jr., Schiffman M. Adding a test for human papillomavirus DNA to cervical-cancer screening. N Engl J Med 2003 Feb 6;348(6):489-90.
(6) Schiffman M, Castle PE, Jeronimo J, Rodriguez AC, Wacholder S. Human papillomavirus and cervical cancer. Lancet 2007 Sep 8;370(9590):890-907.
(7) Mayrand MH, Duarte-Franco E, Rodrigues I, et al. Human papillomavirus DNA versus Papanicolaou screening tests for cervical cancer. N Engl J Med 2007 Oct 18;357(16):1579-88.
(8) Naucler P, Ryd W, Tornberg S, et al. Human papillomavirus and Papanicolaou tests to screen for cervical cancer. N Engl J Med 2007 Oct 18;357(16):1589-97.
(9) Rijkaart DC, Berkhof J, Rozendaal L, et al. Human papillomavirus testing for the detection of high-grade cervical intraepithelial neoplasia and cancer: final results of the POBASCAM randomised controlled trial. Lancet Oncol 2012 Jan;13(1):78-88.
(10) Ronco G, Giorgi-Rossi P, Carozzi F, et al. Efficacy of human papillomavirus testing for the detection of invasive cervical cancers and cervical intraepithelial neoplasia: a randomised controlled trial. Lancet Oncol 2010 Jan 18.
(11) Castle PE, Stoler MH, Wright TC, Jr., Sharma A, Wright TL, Behrens CM. Performance of carcinogenic human papillomavirus (HPV) testing and HPV16 or HPV18 genotyping for cervical cancer screening of women aged 25 years and older: a subanalysis of the ATHENA study. Lancet Oncol 2011 Sep;12(9):880-90.
(12) Sankaranarayanan R, Nene BM, Shastri SS, et al. HPV screening for cervical cancer in rural India. N Engl J Med 2009 Apr 2;360(14):1385-94.
(13) Dillner J, Rebolj M, Birembaut P, et al. Long term predictive values of cytology and human papillomavirus testing in cervical cancer screening: joint European cohort study. BMJ 2008 Oct 13;337:a1754. doi: 10.1136/bmj.a1754.:a1754.
(14) Castle PE, Glass AG, Rush BB, et al. Clinical Human Papillomavirus Detection Forecasts Cervical Cancer Risk in Women Over 18 Years of Follow-Up. J Clin Oncol 2012 Jul 30.
(15) Schiffman M, Castle PE. The Promise of Global Cervical-Cancer Prevention. N Engl J Med 2005;353(20):2101-4.
(16) Denny L, Kuhn L, Hu CC, Tsai WY, Wright TC, Jr. Human papillomavirus-based cervical cancer prevention: long-term results of a randomized screening trial. J Natl Cancer Inst 2010 Oct;102(20):1557-67.
(17) Gustavsson I, Sanner K, Lindell M, et al. Type-specific detection of high-risk human papillomavirus (HPV) in self-sampled cervicovaginal cells applied to FTA elute cartridge. J Clin Virol 2011 Aug;51(4):255-8.
(18) Gustavsson I, Lindell M, Wilander E, Strand A, Gyllensten U. Use of FTA card for dry collection, transportation and storage of cervical cell specimen to detect high-risk HPV. J Clin Virol 2009 Oct;46(2):112-6.
(19) Lenselink CH, de Bie RP, van HD, et al. Detection and genotyping of human papillomavirus in self-obtained cervicovaginal samples by using the FTA cartridge: new possibilities for cervical cancer screening. J Clin Microbiol 2009 Aug;47(8):2564-70.
(20) de Bie RP, Schmeink CE, Bakkers JM, et al. The indicating FTA elute cartridge a solid sample carrier to detect high-risk HPV and high-grade cervical lesions. J Mol Diagn 2011 Jul;13(4):371-6.
(21) Solomon D, Davey D, Kurman R, et al. The 2001 Bethesda System: terminology for reporting results of cervical cytology. JAMA 2002 Apr 24;287(16):2114-9.


